Perkembangan bioteknologi yang pesat saat ini telah menghantarkan umat manusia ke zaman yang serba modern. Berbagai bidang ilmu mulai dari ilmu sosial sampai eksakta mulai mengalami perkembangan yang begitu pesat. Tentu ini menjadi PR besar bagi kita semua untuk mengambil pelajaran akan hal ini. Dengan dihadapkan oleh perkembangan bioteknologi yang begitu pesatnya, maka kita harus menentukan cara-cara dasar apa yang perlu kita tindak lanjuti untuk mengisi era saat ini. Sebuah pekerjaan manusia dalam bidang genetika dan mikrobiologi tentu membutuhkan orang yang ahli di bidangnya. Karena terkait dengan bidang ini kita akan mempelajari bagaimana organisme itu hidup, proses kehidupan mikroba, manfaat serta peranan penting apa yang dapat dimanfaatkan oleh manusia. Salah satunya misalnya rekayasa genetika yang tentu membutuhkan beberapa objek yang harus diperlakukan sesuai prosedur yang ditetapkan.
Bioteknologi membawa kemudahan kepada manusia dalam memanfaatkan binatang dan mikroba uuntuk kepentinga manusia. Kemudahan tersebut digunakan manusia dengan memanfaatkan beberapa binatang dan mikroba yang memiliki kemampuan menghasilkan warna atau bisa memancarkan cahaya (berpendar) dengan warna tertentu. Kemampuan organisme untuk memendarkan dari bagian tubuhnya disebut bioluminescence.
Istilah bioluminescence sering digunakan untuk mendefinisikan kemampuan berpendar ini. Contoh mikroba yang memiliki kemampuan menghasilkan warna adalah Escherichia coli, sedangkan binatang yang memiliki bioluminescence diantaranya firefly (kunang-kunang), jellyfish (ubur-ubur) dan ikan laut-dalam seperti anglerfish. Plankton, gurita dan cumi-cumi tertentu juga memiliki kemampuan berpendar. Sedangkan dari jenis mikroba, bioluminescence dimiliki oleh kebanyakan anggota dari famili Vibrionaceae. Namun perlu diingat bahwasanya kemampuan menghasilkan warna atau pun sifat luminescence tersebut tidak digunakan secara langsung, tetapi melalui teknik isolasi gen yang mengkodenya. Dan telah ditemukan bahwa gen yang mengkode kemampuan menghasilkan warna pada E. coli adalah GUS (beta-glucuronidase), sedangkan kemampuan berpendar pada kunang-kunang dikode oleh LUC (luciferase), dan pada ubur-ubur dikode oleh GFP (green fluorescent protein).
Puluhan ribu protein yang beragam terdapat di dalam tubuh makhluk hidup. Protein-protein ini mengendalikan proses-proses kimia penting secara detail.Bila mesin protein ini malfungsi, biasanya disusul dengan jatuh sakit. Itu sebabnya, biosains merasa perlu memetakan berbagai protein yang ada dalam tubuh. Protein yang semula hanya ditemukan warna hijau itu kini menjadi salah satu alat yang amat bermanfaat di bidang biosains.
Protein warna-warni yang pada awalnya hanya ditemukan warna hijau ini memiliki sebutan GFP atau protein pendar hijau. Protein itu kini menjadi pemandu yang amat penting bagi para ahli biokimia, biologi, ilmuwan kedokteran, dan peneliti-peneliti lainnya. Protein berpendar hijau berperan penting dalam riset kedokteran dan biologi karena memungkinkan para ilmuwan mengetahui bagaimana fungsi organ, penyebaran penyakit, dan respons sel-sel yang terinfeksi terhadap suatu perlakuan.
A. GFP (Green Fluorescent Protein)
 |
| Aequorea victoria |
GFP (Green Fluorescent Protein) adalah pendar cahaya hijau yang merupakan cahaya floresens. Cahaya florsens ini dihasilkan oleh sebuah protein yang bernama Aequorin. Aequorin sebenarnya berasal dari ubur-ubur laut Aequorea victoria. Gen penyandi protein ini dapat dicangkokkan pada genom makhluk hidup dengan proses rekayasa genetika, sehingga makhluk hidup yang telah dimasukkan gen ini akan berpendar hijau.
GFP atau dalam Bahasa Indonesia disebut Protein Pendar Hijau terbentuk dari 238 asam amino, awalnya diisolasi dari ubur-ubur Aequorea victoria yang berpendar hijau ketika disinari cahaya biru. Protein Pendar Hijau (GFP) dari Aequorea victoria memiliki eksitasi utama pada panjang gelombang 395 nm (395 x 10-9 m) dan minor saat 475 nm. Dalam modifikasi untuk membuat biosensor, dan banyak hewan lain telah dibuat bahwa GFP sebagai bukti konsep yang dapat diekspresikan gen melalui organisme yang dibuat. Gen GFP dapat dikenalkan pada organisme dan menjaga genomnya melalui penyilangan, injeksi dengan vektor spiral atau transformasi sel. Sekarang ini, gen GFP telah dikenalkan dan diekspresikan di banyak bakteri, ragi, jamur, lalat, sel mamalia, termasuk manusia.
GFP mengantarkan tiga ilmuan mendapatkan penghargaan Nobel pada tahun 2008 yaitu Oshamu Shimomura, Martin Chalfie, dan Roger Y. Tsien. Oshamu Shimomura memurnikan GFP dan mendeskripsikan sifat biofisik serta proses berpendarnya GFP. Martin Chalfie melaporkan keberhasilannya mengekspresikan gen GFP di dalam sel E. coli dan C. Elegans. Roger Tsien berhasil memodifikasi warna pendaran hijau GFP menjadi bermacam warna yaitu cyan, biru dan kuning dengan cara mengubah satu asam amino pada GFP.
 |
| Gambar pendaran selain warna hijau dari penelitian Tsien |
 |
| Gambar pendaran selain warna hijau dari penelitian Tsien |
Penemuan GFP
Pemurnian dan karakterisasi GFP dari ubur-ubur Aequorea victoria dilakukan pertama kali oleh ilmuwan Jepang bernama Osamu Shimomura pada tahun 1962. Osamu Shimomura yang terdampar di pantai barat Amerika Utara setelah diekstraksikan dari 10.000 ubur-ubur. Bersama rekan-rekan satu timnya menemukan bagian-bagian protein yang bertanggung jawab soal urusan pendar (otomatis bercahaya terutama di kegelapan). Pendar kehijauan itu muncul jika terkena sinar ultraviolet. Namun kegunaannya sebagai alat deteksi biologi molekuler masih belum jelas sampai pada awal tahun 1992. Bagian itu disebut chromophore yaitu sekelompok zat kimia yang mampu menyerap dan memancarkan cahaya.
Gen pewarta transformasi gen dan lokalisasi protein
Tujuan dari pembuatan organisme transgenik yang dapat berpendar pada dasarnya adalah untuk pemantauan suatu proses eksperimen atau biokimia di dalam sel tubuh makhluk hidup.
Untuk proses eksperimen rekayasa genetika misalnya, konfirmasi transformasi dan ekspresi suatu gen asing ke dalam sel inang sangatlah penting. Transformasi adalah proses memasukkan atau mencangkokkan gen asing ke dalam sel makhuk hidup lain, dapat berupa sel bakteri, ragi, tumbuhan, ataupun mamalia.
Bagi para peneliti, sangatlah penting untuk dapat mengetahui dengan cepat, apakah proses transformasi itu telah berlangsung baik atau tidak, dan apakah gen target dapat diekspresikan tanpa masalah. Dari itu, di dalam molekuler biologi dikenal reporter gene atau gen pewarta. Yaitu gen yang dapat memberitahukan dengan jelas pada para peneliti bahwa proses transformasi telah berjalan dengan sukses. Gen yang menghasilkan protein yang dapat berpendar hijau atau GFP inilah yang banyak dipakai oleh para ilmuwan sebagai gen pewarta.
Gen asing target yang ingin dicangkokkan ke dalam suatu sel organisme biasanya digabungkan dengan gen GFP dalam bentuk gen kimera atau gen gabungan, sehingga nanti akan dihasilkan protein baru fungsional (yang menjadi sifat baru organisme tersebut) dalam bentuk protein gabungan dengan GFP. Jadi, jika gen yang digabung dengan gen pewarta berhasil masuk dan fungsional di dalam sel bakteri E. coli misalnya, maka sel E. coli yang berpendar hijau di kegelapan adalah bakteri transgenik yang fungsional yang membawa sifat baru. Proses penapisan klon transgenik yang positif menjadi lebih cepat dan mudah.
Dibandingkan dengan gen pewarta lain yang kebanyakan enzim yang memerlukan substrat untuk menghasilkan warna atau pendar cahaya, GFP adalah gen pewarta yang menarik sekaligus mudah dalam hal visualisasi, karena untuk berpendar GFP sama sekali tak memerlukan substrat. GFP menghasilkan sinar hijau fluoresens secara instrinsik, ketika diberi sinar eksitasi pada panjang gelombang biru sekitar 395 nanometer. Jadi hanya dibutuhkan lampu UV gelombang panjang atau sinar biru untuk dapat mendeteksinya dalam kegelapan.
GFP juga menjadi gen pewarta idola dalam hal pencitraan proses tracking atau lokalisasi suatu protein. Karena tidak perlu penambahan substrat dan mudah divisualisasi, GFP dapat diaplikasikan untuk memantau jejak protein, kapan dan dimana suatu gen terinduksi menjadi suatu protein, dalam kondisi sel masih hidup.
Tak hanya berpendar hijau
GFP adalah protein yang merupakan polimer dari 238 asam amino dengan berat molekul sekitar 27 Kilo Dalton. Di dalam protein ini ada gugus yang disebut chromophore yang berperan sangat penting dalam proses perpendaran hijau. Chromophore ini adalah kelompok tiga residu asam amino di posisi 65 (Serin), 66 (Tirosin), dan 67 (Glisin). Ketika dikenai energi cahaya biru atau UV maka pada gugus ini akan terjadi reaksi oksidasi. Energi yang diserap membuat elektronelektron di dalam gugus ini tereksitasi dan menghasilkan energi yang lebih rendah yaitu energi cahaya hijau.
Pengetahuan para ilmuwan yang lengkap tentang molekuler dan struktur dari GFP ini membuat para ilmuwan dapat merekayasa protein ini menjadi beberapa mutan. Sekarang tidak hanya protein yang dapat berpendar hijau yang digunakan sebagai gen pewarta. Tetapi juga protein berpendar biru, merah, atau kuning berhasil ditemukan oleh para ilmuwan sebagai turunan dari GFP.
Ilmuwan mengganti asam amino di gugus chromophore dengan asam amino lain dengan proses mutasi gen. Misalnya asam amino ke 66 (Tirosin) disubstitusi dengan asam amino Histidin, mutasi ini menyebabkan protein menghasilkan warna pendar biru bukan hijau. Subtitusi asam amino ke 203 (Treonin), yang posisinya dalam kristal GFP dekat chromophore, dengan Tirosin menghasilkan protein yang berpendar kuning. Gen pewarta turunan GFP yang menghasilkan berbagai pendar warna ini memudahkan para peneliti untuk melakukan pemantauan beberapa proses biokimia secara bersamaan, sehingga informasi yang diperoleh dapat lebih cepat dan lebih lengkap. Karena sinar UV relatif berbahaya untuk sel makhluk hidup, maka para ilmuwan juga merekayasa protein ini (juga dengan proses mutasi gen), sehinga hanya dapat dieksitasi oleh energi cahaya gelombang panjang. Dengan demikian proses deteksi transformasi ataupun tracking tidak berbahaya bagi sel makhluk hidup, karena tidak perlu terpapar dengan sinar UV.
GFP menjadi istimewa karena bersifat auto-katalitik, tidak membutuhkan kofaktor atau enzim lain agar ia bekerja. Selain itu GFP dapat digabung (fusi) dengan protein lain tanpa saling mengganggu fungsi masing-masing. Sehingga GFP dapat digunakan secara luas di berbagai organisme.
Pendaran GFP dapat diamati secara visual dengan bantuan mikroskop. Berikut ini beberapa teknik dalam aplikasi GFP, antara lain:
a) Fusi Translasi
b) Fusi Transkripsi
c) FLIP dan FRAP
a) Fusi Translasi
Teknik pertama dikenal dengan fusi translasi, dimana ORF (Open Reading Frame) GFP diklon di belakang ORF gen yang akan kita amati, sehingga nanti akan ditranslasi menjadi sebuah protein gabungan yang panjang. Jadi jika kita melihat pendaran GFP maka berarti protein yang kita amati pun terekspresi di situ. Cahaya fluorescent GFP dapat diamati dalam bentuk gambar diam maupun bergerak sehingga kita dapat mengetahui lokasi dan pergerakan protein di dalam sel.
b) Fusi Transkripsi
Teknik kedua disebut fusi transkripsi dimana ekspresi gen yang kita amati dan GFP digerakkan melalui promoter yang sama tetapi antara kedua gen tersebut diselingi oleh stop kodon, jadi ekspresinya berbarengan namun tetap menghasilkan dua protein terpisah. Dalam hal ini sel yang mengekspresikan gen pertama akan dipenuhi oleh GFP yang larut sehingga berpendar, dan bisa mendeteksi sel mana yang mengekspresikannya.
c) FLIP dan FRAP
Kita tahu bahwa suatu molekul mengemisikan cahaya fluorescent ketika tereksitasi, namun kondisi ini tidak berlangsung selamanya, dalam jangka waktu tertentu cahayanya akan redup dan padam. FLIP dan FRAP ini digunakan untuk mempelajari dinamika protein yang terlabel GCFP. Caranya dengan bleach-out (memadamkan) daerah tertentu pada sel, kemudian dilihat berapa lama waktu yang diperlukan oleh protein terlabel protein untuk “merembes” kembali ke area gelap tadi, teknik ini yang disebut FRAP (Fluorescent Recovery After Photobleaching). Kita juga dapat mengamati seberapa besar penurunan intensitas fluorescent secara keseluruhan di bagian sel yang lain ketika protein yang sudah di-photobleach tadi terdifusi, atau disebut FLIP (Fluorescent Loss in Photobleaching).
d) FRET
FRET atau fluorescence resonance energy transfer sudah banyak diaplikasikan dalam beberapa teknik seperti Real Time PCR. Prinsipnya yaitu dengan memanfaatkan dua buah fluophore (zat yang dapat ber-fluorescent) yang mana fluorophore pertama memiliki spektrum emisi yang tumpang tindih dengan spektrum eksitasi fluorophore kedua. Jadi ketika fluorophore pertama memancarkan cahaya fluorescent, otomatis yang kedua pun akan tereksitasi dan memancarkan fluorescent. Dalam aplikasinya, dua buah protein dilabel dengan dua macam GFP yang memenuhi kriteria FRET tadi. Kemudian sel ditembak dengan laser yang dapat mengeksitasi hanya fluorophore pertama. Dengan demikian jika protein kedua ada dekat dengan protein pertama, otomatis akan terdeteksi juga karena memancarkan cahaya yang berbeda.
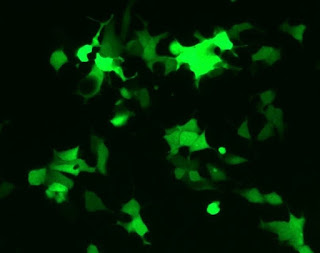 |
| Sel yang mengekspresikan GFP |
Manfaat GFP
Teknologi yang menggunakan GFP ini membantu kita menyaksikan pertumbuhan tumor ganas kanker, perkembangan penyakit Alzheimer pada otak, atau perkembangan bakteri patogenik. Bayangkan, dengan GFP kita mampu mengikuti pertumbuhan sel-sel secara individu, padahal tubuh kita terdiri dari triliunan sel dengan beragam tugas dan fungsinya.
Douglas Prasher melaporkan keberhasilannya dalam mengkloning dan mendapatkan sekuen nukleotida GFP. Keberhasilan kloning tersebut dilanjutkan dengan aplikasi GFP pada dua sistem organisme prokaryotik (bersel tunggal) dan eukaryotik (multi sel/organisme tingkat tinggi). Organisme prokaryotik yang digunakan adalah Escherichia coli, sedangkan organisme eukaryotiknya adalah cacing dari filum Nematoda (cacing gelang) yaitu Caenorhabditis elegans. Hasilnya sangat memuaskan. Ekspresi GFP cukup stabil pada kedua sistem tersebut.
Akhir-akhir ini, GFP fusion system digunakan untuk mengetahui ekspresi (localization) suatu gen dengan menggunakan onion epidermal cells atau protoplast. Pada umumnya promoter yang dipakai untuk GFP fusion adalah 35S sehingga konstruk akhir menjadi p35S:gen/cDNA:GFP. Ekspresi yang muncul tersebut sering disebut dengan transient expression dari suatu gen.
Adapun Chalfie yang lahir pada 1947 lalu adalah seorang profesor biologi di Universitas Columbia, AS. Ia melanjutkan apa yang telah dimulai Shimomura. Chalfie membantu penemuan gen yang mengendalikan GFP dan menemukan cara untuk memasukkan gen tersebut ke tubuh Caenorhabditis elegans atau cacing gelang. Idenya adalah menghubungkan gen GFP dengan berbagai pemicu gen akan memungkinkan dirinya melihat di mana protein-protein yang berbeda dihasilkan.
Dalam satu dekade terakhir, GFP telah berfungsi sebagai bintang pembimbing bagi ahli biokimia, ahli biologi, ilmuwan kedokteran, dan peneliti-peneliti lainnya. Protein ini telah menjadi salah satu dari alat yang paling penting yang digunakan dalam biosains kontemporer.
Penelitian lanjutan atas GFP telah berhasil dimanfaatkan sebagai alat pencari dan pengikat pada biosains. Dengan menggunakan teknologi deoxyribo nucleic acid (DNA), para ilmuwan tersebut mampu menghubungkan GFP pada protein-protein lainnya. Gen untuk menciptakan GFP disuntikkan ke dalam DNA hewan-hewan percobaan, bakteri, atau sel-sel lainnya. Protein tersebut akan berpendar di bawah paparan sinar ultraviolet.
Para peneliti memanfaatkan GFP untuk mengamati proses-proses dalam tubuh yang semula tak terlihat. Misalnya, perkembangan sel-sel saraf di dalam otak atau bagaimana penyebaran sel kanker. Bahkan kini para peneliti dapat mengikuti “nasib” berbagai jenis sel dengan bantuan GFP. Misalnya, sel saraf yang rusak pada penyakit Alzheimer, atau bagaimana sel beta penghasil insulin terbentuk di pankreas saat pertumbuhan embrio (bakal bayi).
Para peneliti menciptakan brainbow, yakni mereka berhasil memberi warna yang berubah-ubah pada sel-sel saraf yang berlainan dalam otak seekor tikus.
 |
| Sel yang mngekspresikan GFP pada otak tikus |
Warna-warna selain hijau ditemukan Roger Y Tsien. Dia juga menemukan penjelasan mengapa GFP bisa bersinar di kegelapan (fluorescents). Tsien lalu melengkapi tahap terakhir penelitian. Dengan menggunakan teknologi DNA, profesor di Universitas California itu menukar beragam asam amino di dalam bagian-bagian yang berbeda GFP. Hal itu memungkinkan protein menyerap dan mengeluarkan cahaya. Pria yang lahir 56 tahun lalu itu kemudian mengembangkan varian baru GFP yang dapat berpendar lebih terang dan dengan warna yang berlainan.
B. Transgenik
Transgenik terdiri dari kata trans yang berarti pindah dan gen yang berarti pembawa sifat. Jadi transgenik adalah memindahkan gen dari satu makhluk hidup ke makhluk hidup lainnya, baik dari satu tanaman ketanaman lainnya, atau dari gen hewan ke tanaman.
Transgenik secara definisi adalah the use of gene manipulation to permanently modify the cell or germ cells of organism (penggunaan manipulasi gen untuk mengadakan perubahan yang tetap pada sel makhluk hidup).
Tujuan memindahkan gen tersebut untuk mendapatkan organisme baru yang memiliki sifat lebih baik. Hasilnya saat ini sudah banyak jenis tanaman transgenik, misalnya jagung, kentang, kacang, kedelai, dan kapas. Keunggulan dari tanaman transgenik tersebut umumnya adalah tahan terhadap serangan hama. Rekayasa genetika seperti dalam pembuatan transgenik dilakukan untuk kesejahteraan manusia.
Organisme transgenik adalah organisme yang mendapatkan pindahan gen dari organisme lain. Gen yang ditransfer dapat berasal dari jenis (spesies) lain seperti bakteri, virus, hewan, atau tanaman lain. Transgenik dapat dilakukan pada tanaman maupun hewan.
Hewan transgenik merupakan hewan yang diinjeksi dengan DNA dari hewan lain. Transformasi gen tersebut yang umumnya berasal dari spesies yang sama, tapi dapat juga berasal dari spesies berbeda yang dilakukan terhadap embrio sebelum hewan transgenik tersebut dilahirkan. Transformasi genetik diharapkan menyebabkan mutasi spontan sehingga genetik dari hewan yang ditransformasi termodifikasi sesuai dengan gen yang diharapkan muncul sebagai performans.
Transfer gen ini dapat dilakukan dengan beberapa metode, yaitu metode senjata gen, metode transformasi DNA yang diperantarai bakteri Agrobacterium tumefaciens, dan elektroporasi (metode transfer DNA dengan bantuan listrik).
 |
| Gambar skematik transgenik pada tikus |
Untuk melakukannya, digunakan senjata yang dapat menembakkan mikro-proyektil berkecepatan tinggi ke dalam sel makhluk hidup lain. Mikro-proyektil tersebut akan mengantarkan DNA untuk masuk ke dalam sel tanaman. Penggunaan senjata gen memberikan hasil yang bersih dan aman, meskipun ada kemungkinan terjadi kerusakan sel selama penembakan berlangsung.
 |
| Gambar proses mikroinjeksi |
Bakteri Agrobacterium tumefaciens dapat menginfeksi tanaman secara alami karena memiliki plasmid Ti, suatu vektor (pembawa DNA) untuk menyisipkan gen asing. Di dalam plasmid Ti terdapat gen yang menyandikan sifat virulensi untuk menyebabkan penyakit tanaman tertentu. Gen asing yang ingin dimasukkan ke dalam tanaman dapat disisipkan di dalam plasmid Ti. Selanjutnya, A. tumefaciens secara langsung dapat memindahkan gen pada plasmid tersebut ke dalam genom (DNA) tanaman. Setelah DNA asing menyatu dengan DNA tanaman maka sifat-sifat yang diinginkan dapat diekspresikan tumbuhan.
3) Metode elektroporasi.
Pada metode elektroporasi ini, sel diberi kejutan listrik dengan voltase tinggi untuk membuka pori-pori membran sel sehingga DNA asing dapat masuk ke dalam sel dan bersatu (terintegrasi) dengan DNA kromosom. Setelah proses transfer DNA selesai, dilakukan seleksi sel untuk mendapatkan sel yang berhasil disisipi gen asing.
C. Manfaat Hewan Transgenik Fluorescent
Hewan transgenik merupakan hewan yang diinjeksi dengan DNA dari hewan lain. Transformasi gen tersebut yang umumnya berasal dari spesies yang sama, tapi dapat juga berasal dari spesies berbeda yang dilakukan terhadap embrio sebelum hewan transgenik tersebut dilahirkan. Transformasi genetik diharapkan menyebabkan mutasi spontan sehingga genetik dari hewan yang ditransformasi termodifikasi sesuai dengan gen yang diharapkan muncul sebagai performans.
Hewan transgenik dikembangkan dengan 3 cara, yaitu mikroinjeksi DNA, transfer gen dengan media retrovirus dan transfer gen dengan media sel cangkokan embrionik. Mikroinjeksi DNA dilakukan dengan melakukan injeksi langsung gen terpilih yang diambil dari anggota lain dalam spesies yang sama ataupun berbeda ke dalam pronukleus ovum yang telah dibuahi. Transfer gen dengan media retrovirus menggunakan retrovirus sebagai vector, kemudian menginjeksikan DNA ke dalam sel inang. DNA dari retrovirus berintegrasi ke dalam germ untuk bekerja. Transfer gen dengan media sel cangkokan embrionik diaplikasikan dengan menggunakan sequence DNA yang diharapkan muncul ke dalam kultur in vitro sel cangkokan embrionik. Sel cangkokan dapat menjadi organisme lengkap. Sel kemudian berikatan dalam embrio pada tahap perkembangan blastosit (Bains, 1993).
Hewan yang telah berhasil dikembangkan menjadi hewan transgenik adalah mencit sebagai hewan pioneer yang pertama kali dibuat. Saat ini telah dikembangkan ke tikus, kelinci, domba, sapi dan babi. Salah satu tujuan dilakukan manipulasi genetik adalah untuk menghasilkan hewan yang memiliki karakter yang diharapkan (breeding).
Manipulasi genetik dilakukan untuk beberapa tujuan. Pada bidang pertanian, dengan manipulasi genetik dihasilkan hewan yang memiliki karakter yang diharapkan (breeding), pangan yang lebih sehat dihasilkan lebih cepat (kualitas pangan) dan resistensi terhadap infeksi bakteri yang tersebar bebas (resistensi penyakit). Bidang industri, produk baru (kambing yang menghasilkan sutra laba-laba) dapat diciptakan. Dalam bidang riset, memunculkan model riset baru (mencit transgenik) dan evolusi yang dipaksa (organisme baru dengan karakter yang lebih diharapkan).
 |
| Gambar tikus transgenic flourescent |
Meskipun banyak potensi dan manfaat yang dapat diambil dari hewan transgenik, akan tetapi proses yang dilibatkan dalam pengembangan hewan transgenik di laboratorium berpotensi atau memiliki dampak yang buruk terhadap masa depan hewan yang dilibatkan. Proses yang terjadi dalam pengembangan galur transgenik baik di laboratorium maupun di hewan ternak secara potensial memiliki dampak utama terhadap hewan yang diamati. Area tertentu dimana masalah dapat terjadi adalah pada proses eksperimental yang berhubungan dengan produksi in vitro dan transfer embrio serta selama gestasi dan kelahiran hewan yang dimanipulasi. Pada hewan ternak, dibandingkan dengan IB, prosedur yang digunakan sebelum dan sesudah mikroinjeksi (contohnya kultur in vitro dan transfer embrio) mungkin memperpanjang gestasi, meningkatkan bobot lahir dan menyebabkan insiden kesulitan lahir dan kehilangan prenatal yang lebih tinggi.



2 komentar
Write komentarkak.. ada dapusnya?
Replyada dapusnya, tapi belum sempet keupload :D
ReplyEmoticonEmoticon